Pengertian Serta Contoh Isotop, Isobar dan Isoton – Dalam ilmu kimia dasar, kita akan menjumpai tiga istilah yakni isotop, isobar dan isoton. Apa itu? Apa maknanya?. Nah, di halaman ini kita akan membahas ketiga istilah tersebut beserta teladan dan fungsinya.
Pembahasan perihal isotop, isobar dan isoton merupakan pembahasan dasar dalam ilmu kimia yang kita masukan dalam Bab 01 struktur atom. Silahkan buka kategori tersebut di dalam situs ini kalau ingin melihat pembahasan sebelumnya.
A. Isotop
Pengertian isotop: Atom-ataom yang mempunyai nomor atom yang sama namun mempunyai nomor massa yang berbeda. Dengan kata lain sebuah unsur yang mempunyai jumlah proton dan elektron sama sanggup mempunyai jumlah neutron yang berbeda, itulah yang dinamakan dengan isotop.
Contoh isotop dalam atom:
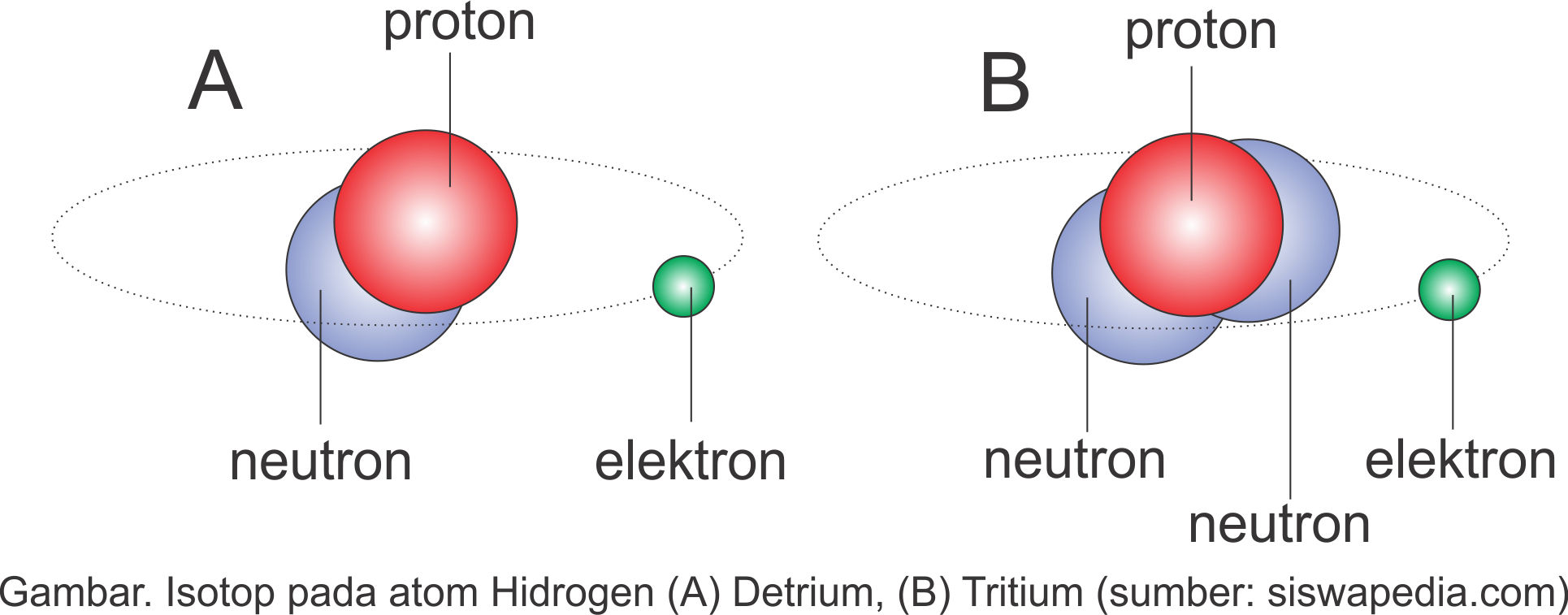
Hidrogen mempunyai isotop 1H1, 2H1 (detrium) dan 3H1 (tritium)
Oksigen mempunyai isotop 16O8, 17O8 dan 18O8
Karbon mempunyai isotop 12C6, 13C6 dan 14C6
Nitrogen mempunyai isotop 14N7 dan 15N7
Helium mempunyai isotop 3He2 dan 4He2
Klorin mempunyai isotop 35Cl17 dan 37Cl17
Besi mempunyai isotop 54Fe26, 55Fe26, 56Fe26,57Fe26 dan 58Fe26
Neon mempunyai isotop 20Ne10, 21Ne10 dan 22Ne10
Natrium mempunyai isotop 22Na11, 23Na11 dan 24Na11
Belerang mempunyai isotop 32S16, 33S16, 34S16 dan 36S16
Coba perhatikan sepuluh unsur di atas, meskipun nomor atomnya sama mereka sanggup mempunyai nomor massa yang berbeda. Nomor atom yakni jumlah proton sedangkan nomor massa merupakan jumlah proton dan elektron. Silahkan lihat kepingan sebelumnya.
Kegunaan Isotop dalam kehidupan
- Fe-59 sanggup dipakai untuk mengukur laju pembentukan sel darah merah di dalam tubuh
- Na-24 sanggup dipakai untuk mendeteksi kebocoran pipa di dalam tanah, caranya Na-24 dilarutkan dalam air/minyak lalu dengan memakai detektor akan diketahui kebocorannya. Yang bocor niscaya radiasinya lebih banyak. Selain itu juga sanggup dipakai untuk mempelajari peredaran darah manusia.
- P-32 sanggup dipakai untuk mendeteksi pemakaian pupuk pada tanaman-tanaman.
- CO-60 sanggup dipakai untuk pengobatan kanker.
- I-131 sanggup dipakai untuk mendeteksi kelainan pada kalenjar tiroid.
- C-14 daat dipakai untuk mengetahui kecepatan pembentukan senyawa pada proses fotosintesis. Selain itu, juga dipakai untuk memilih usia fosil atau benda-beda bersejarah. Caranya dengan melihat waktu paruh-nya.
- O-18 sanggup dipakai untuk mengetahui perubahan asam karboksilat dan alkohol menjadi suatu ester (dengan memakai asam sebagai katalisnya). Ini dinamakan proses esterifikasi.
B. Isobar
Pengertian Isobar: unsur atomnya berbeda namun mempunyai nomor massa yang sama. Hal ini dinamakan isobar.
Contoh Isobar
Natrium dan Magnesium sanggup mempunyai nomor massa yang sama yaitu 24Na11 dan 24Mg12
Hidrogen dan Helium sanggup mempunyai nomor massa yang sama yaitu 3H1 dan 3He2
Karbon dan Nitrogen sanggup mempunyai nomor massa yang sama yaitu 14C6 dan 14N7
C. Isoton
Pengertian Isoton: Unsur berbeda namun mempunyai jumlah neutron yang sama.
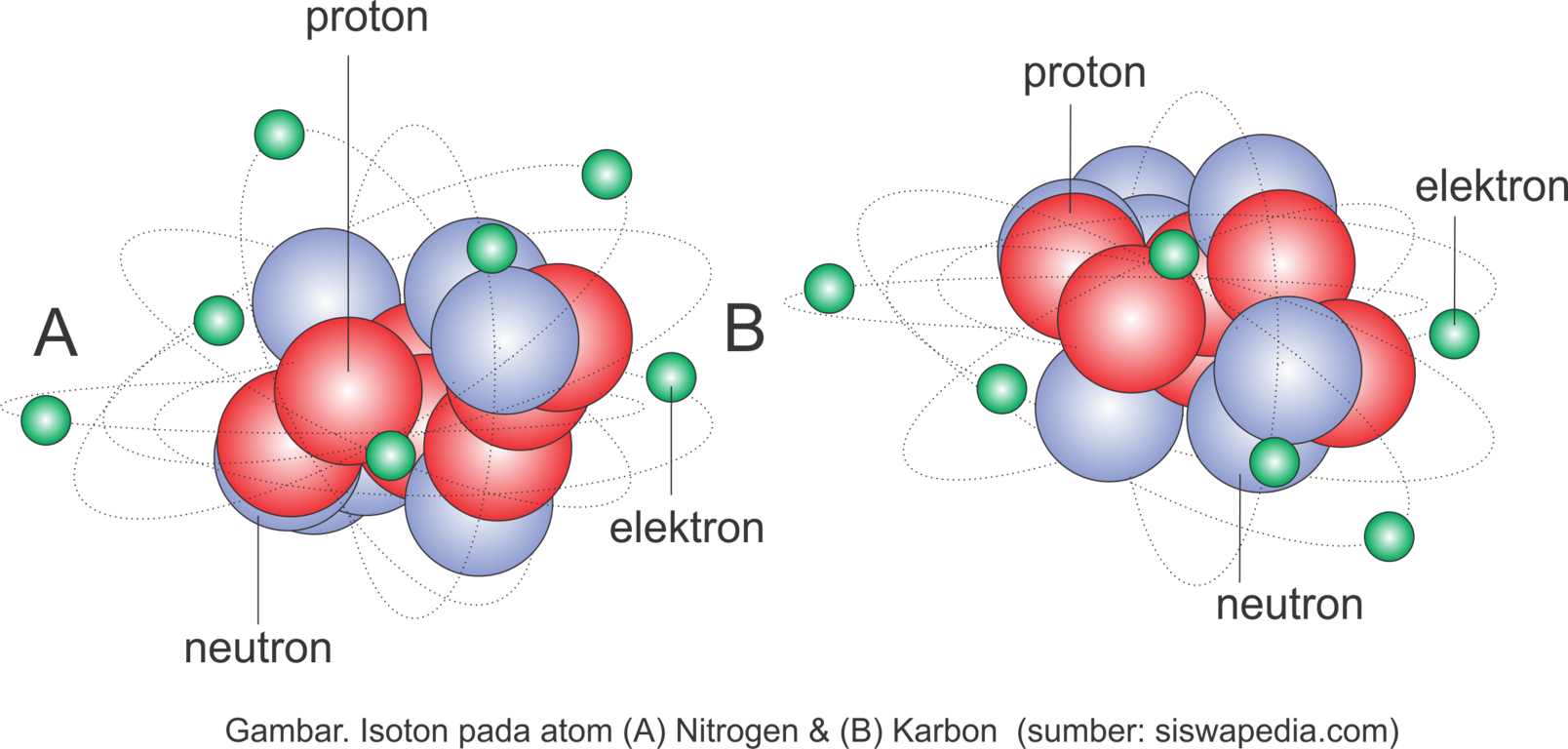
Contoh Isoton
Hidrogen (3H1) dan Helium (3He2) mempunyai jumlah neutron sama yaitu 2.
Argon (40Ar18) dan Kalsium (42Ca20) mempunyai jumlah neutron sama yaitu 22.
Nitrogen(14N7) dan Karbon (13C6) mempunyai jumlah neutron sama yaitu 7.
Natrium (23Na11) dan Magnesium (24Mg12) mempunyai jumlah neutron sama yaitu 12.
Kalium (39K19) dan Kalsium (40Ca20) mempunyai jumlah neutron sama yaitu 20.
Daftar Pustaka
Harnanto, Arie dan Ruminten. 2009. Kimia I. Jakarta: Pusat Perbukuan Departemen Pendidikan Nasional.
Ratna dkk. 2008. Kimia Jilid 1. Jakarta: Direktorat Pembinaan Sekolah Menengah Kejuruan.
Sumber https://www.siswapedia.com