Teori Atom – Tentu kalian sudah tidak ajaib dengan bahan yang akan kami bahas kali ini. Karena, kalian niscaya sering menemui bahan teori atom ini pada mata pelajaran fisika. Materi ini juga pastinya ini bukan lah bahan yang gampang. Nah, pada pembahasan kali ini kita akan membahas wacana teori atom berdasarkan para mahir dan gambarnya.
Pengertian dan Asal-Usul Teori Atom
Sebelum membahas wacana bahan teori atom berdasarkan para ahli, kita perlu mengetahui terlebih dahulu wacana pengertian dan asal-usul teori atom. Kata atom berasal dari kata ”atomos” dalam bahasa Yunani yang mempunyai arti ”tidak sanggup dibagi”.
Awal mula teori dasar atom dikemukakan oleh spesialis dari Yunani yaitu Democritus pada kurun ke-4 SM. Menurut teori atom yang dikemukakan oleh Democritus, atom yakni suatu benda yang sangat kecil hingga tidak sanggup dibagi-bagi lagi.
Menurut ia atom sepenuhnya padat, ada ruang kosong antar atom untuk menunjukkan ruang untuk pergerakannya (seperti pergerakan dalam air dan udara), dan tidak mempunyai struktur internal.
Akan tetapi, model teori atom Democritus ini kurang mempunyai bukti eksperimental hingga mulai tahun 1800an muncul teori-teori gres berdasarkan hasil eksperimen. Adapun beberapa teori atom yang muncul dan paling populer dalam ilmu Fisika ketika ini yaitu teori atom berdasarkan Rutherford, John Dalton, dan JJ. Thomson.
Teori Atom John Dalton
Pada tahun 1803, John Dalton mengemukanan teori atom didasarkan pada dua hukum, yaitu aturan susunan tetap (hukum prouts) dan aturan kekekalan massa (hukum Lavoisier).
Menurut Prouts: “Perbandingan massa unsur-unsur dalam suatu senyawa selalu tetap.”
Menurut Lavosier: “Massa total zat-zat sebelum reaksi akan selalu sama dengan massa total zat-zat hasil reaksi”.
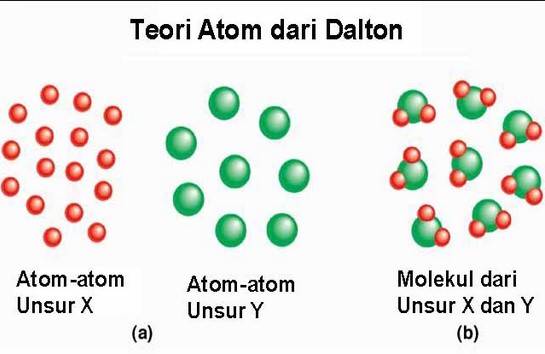 Berdasarkan dari kedua aturan tersebut, john Dalton mengemukakan pendapatnya wacana teori atom sebagai berikut:
Berdasarkan dari kedua aturan tersebut, john Dalton mengemukakan pendapatnya wacana teori atom sebagai berikut:
- Atom yakni pecahan terkecil dari bahan yang tidak sanggup dibagi-bagi lagi.
- Atom digambarkan sebagai bola pejal yang mempunyai ukuran sangat kecil.
- Atom-atom bergabung dan terbentuk senyawa. Misalnya air terdiri atom-atom hidrogen dan atom-atom oksigen.
Reaksi kimia yakni suatu pemisahan atau penyusunan kembali dari atom-atom, sehingga atom tersebut tidak akan sanggup diciptakan atau dimusnahkan.
Kelebihan:
Mulai membangkitkan minat terhadap penelitian mengenai model atom.
Kelemahan:
Teori atom berdasarkan Dalton ini belum bisa menerangkan bahwa larutan sanggup menghantarkan arus listrik.
Baca Juga:
Model Teori Atom JJ. Thomson
Menurut J.J. Thomson pada tahun 1900, menurutnya di dalam atom terdapat partikel elektron dan proton. Berdasarkan hasil eksperimen yang telah dilakukannya, proton mempunyai massa yang lebih besar dibandingkan dengan elektron, sehingga model atom Thomson sanggup digambarkan sebagai proton tunggal yang besar.
Proton mempunyai electron-elektron yang sanggup menetralkan muatan nyata pada proton. Menurut JJ. Thomson, atom terdiri dari bulatan yang bermuatan nyata yang rapat muatan. Secara umum teori atom thomson berbunyi: “Atom yakni suatu bola pejal yang mempunyai muatan nyata dan di dalamya tersebar muatan negatif elektron.”
 Secara sederhana model teori atom thomson sanggup dianalogikan menyerupai jambu biji yang telah dikupas kulitnya. Nah, Biji jambu yang tersebar merata ini dimodelkan sebagai suatu electron sedangkan bulatan daging jambu yang pejal dianalogikan sebagai proton.
Secara sederhana model teori atom thomson sanggup dianalogikan menyerupai jambu biji yang telah dikupas kulitnya. Nah, Biji jambu yang tersebar merata ini dimodelkan sebagai suatu electron sedangkan bulatan daging jambu yang pejal dianalogikan sebagai proton.
Kelebihan:
Teori atom Thomshon bisa pertanda bahwa adanya partikel lain yang bermuatan negatif di dalam atom. Berarti atom bukanlah pecahan terkecil pada suatu unsur.
Kelemahan:
Model Thomson ini tidak bisa menjelaskan susunan muatan negatid dan nyata yang terdapat dalam bola atom tersebut.
Model Atom Rutherford
Menurut Rutherford Pada tahun 1910 bersama dua orang muridnya (Hans Geiger dan Erners Masreden) melaksanakan percobaan yang dikenal dengan hamburan sinar alfa (λ) terhadap lempeng tipis emas. Dari hasil pengamatannya ditemukan bahwa sebagian besar partikel alfa bisa menembus lembaran emas tanpa dibelokkan.
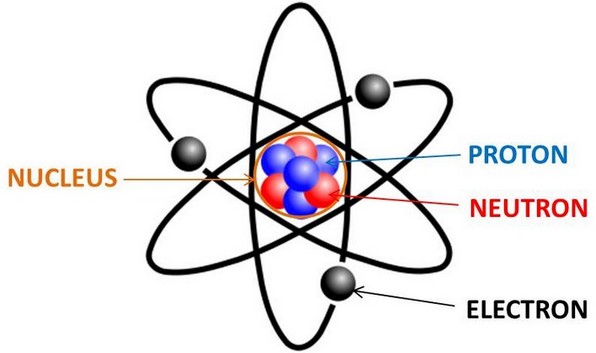 Berdasarkan gejala-gejala yang terjadi, Rutherford menciptakan kesimpulan bahwa:
Berdasarkan gejala-gejala yang terjadi, Rutherford menciptakan kesimpulan bahwa:
- Atom bukanlah sebuah bola pejal, sebab hampir semua partikel alfa diteruskan.
- Jika suatu lempeng emas dianggap sebagai suatu lapisan atom emas, maka di dalam atom emas tersebut terdapat partikel yang kecil yang mempunyai positif.
- Partikel tersebut yakni partikel yang menyusun inti atom.
Berdasarkan dari hasil pengamatannya tersebut, Rutherford mengemukan sebuah model atom yaitu ”Atom terdiri dari inti atom yang sangat kecil serta mempunyai muatan positif, serta dikelilingi oleh elektron bermuatan negatif.”
Kelebihan:
Atom tersusun terdiri dari inti atom dan elektron yang mengelilingi inti atom tersebut.
Kelemahan:
Teori ini tidak sanggup menjelaskan mengapa suatu elektron tidak sanggup jatuh ke dalam inti atom.
Model Atom Niels Bohr
Menurut Neils Bohr pada tahun 1913, ia memperbaiki kegagalan atom Rutherford melalui percobaannya wacana spektrum atom hidrogen. Berdasarkan hasil percobaannya Bohr menunjukkan citra keadaan orbit elektron dalam menempati kawasan di sekitar inti atom. Menurut Neils Bohr, elektron hanya mengelilingi inti atom pada orbit tertentu saja, yaitu hanya terdapat orbit dalam jumlah tertentu saja dan perbedaan antar orbit tersebut yakni jarak orbit ke inti atom.
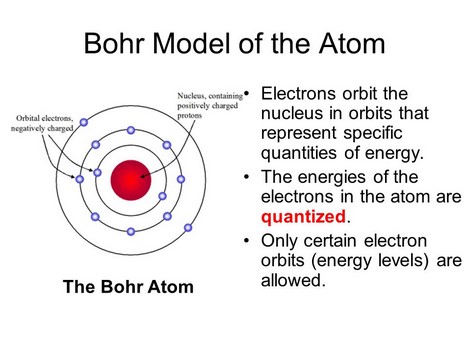 Penjelasan Niels Bohr wacana atom merupakan campuran antara teori klasik dari teori kuantum Planck dan Rutherford. Secara garis umum, Niels Bohr mengemukaan model atom sebagai berikut:
Penjelasan Niels Bohr wacana atom merupakan campuran antara teori klasik dari teori kuantum Planck dan Rutherford. Secara garis umum, Niels Bohr mengemukaan model atom sebagai berikut:
- Elektron dalam atom bergerak mengelilingi inti atom pada lintasan tertentu, serta tidak memancarkan energi.
- Elektron dalam atom sanggup berpindah antar lintasan.
- Perpindahan elektron dalam atom yaitu dari tingkat energi tertinggi ke tingkat terrendah disertai pemancaran energi.
Menurut model teori atom Bohr, elektron-elektron mengelilingi inti pada lintasan-lintasan tertentu yang disebut sebagai tingkat energi atau kulit elektron. Tingkat energi paling rendah yaitu kulit elektron yang terletak dibagian paling dalam, semakin keluar semakin besar nomor kulit electron tersebut dan semakin tinggi pula tingkat energinya.
Kelebihan:
Atom Bohr yakni suatu atom yang terdiri dari beberapa kulit sebagai tempat berpindahnya suatu elektron.
Kelemahan:
Model atom ini yakni tidak bisa menjelaskan efek Strack dan efek Zeeman.
Nah, itulah klarifikasi mengenai teori atom berdasarkan para mahir dan gambarnya yang sanggup kami berikan. Jika kalian sudah sanggup memahami bahan ini kalian sanggup melanjutkan ke bahan yang selanjutnya yaitu Struktur Atom. Terimakasih telah berkunjung dan biar sanggup bermanfaat.
Sumber https://rumusrumus.com